Dnes je 19. dubna 2024 15:22:23
Vodík
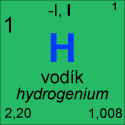
Vlastnosti
chemická značka H (lat. Hydrogenium) je nejlehčí a nejjednodušší
plynný chemický prvek, tvořící převážnou část hmoty ve vesmíru.
Má široké praktické využití jako zdroj energie, redukční činidlo v
chemické syntéze nebo metalurgie nebo náplň balonů a vzducholodí.
Základní fyzikálně-chemické vlastnosti
Vodík je bezbarvý, lehký plyn, bez chuti a zápachu. Je značně reaktivní, především s kyslíkem a halogeny se slučuje velmi bouřlivě i když pro spuštění této reakce je nutná inicializace (např. jiskra, která zapálí kyslíko-vodíkový plamen).
Vodík vytváří sloučeniny se všemi prvky periodické tabulky s výjimkou vzácných plynů, zejména pak s uhlíkem, kyslíkem, sírou a dusíkem, které tvoří základní stavební jednotky života na Zemi.
Vodík je schopen tvořit zvláštní typ chemické vazby, nazývaný vodíková vazba nebo také vodíkový můstek, kdy vázaný atom vodíku vykazuje afinitu i k dalším atomům, s nimiž není poután klasickou chemickou vazbou. Mimořádně silná je vodíková vazba s atomy kyslíku, což vysvětluje anomální fyzikální vlastnosti vody (vysoký bod varu a tání atd.).
Objevil jej roku 1766 Angličan Henry Cavendish.
Výskyt v přírodě
Elementární vodík je na Zemi přítomen jen vzácně. Plynný vodík se v našem prostředí vyskytuje ve formě dvouatomových molekul H
2, je však známo, že v mezihvězdném prostoru je přítomen z převážné části jako atomární vodík H. V zemské atmosféře se vyskytuje jen ve vyšších vrstvách a díky své mimořádně nízké hmotnosti postupně z atmosféry vyprchává. Elementární vodík je však jednou z podstatných složek zemního plynu, vyskytuje se i v ložiscích uhlí.
Ze sloučenin je nejvíce zastoupena voda, která jako moře a oceány pokrývá 2/3 zemského povrchu.
Další významný zdroj vodíku představují organické sloučeniny. Vodík patří společně s uhlíkem, kyslíkem a dusíkem mezi tzv. biogenní prvky, které tvoří základní stavební kameny všech živých organizmů. Díky tomu se vodík vyskytuje prakticky ve všech sloučeninách tvořících nejvýznamnější surovinu současné energetiky a organické chemie – ropu.
Vodík je základním stavebním prvkem celého vesmíru, vyskytuje se jak ve všech svítících hvězdách, tak v mezigalaktickém prostoru. Podle současných měření se podílí ze 75 % na hmotě a dokonce z 90 % na počtu atomů přítomných ve vesmíru.
Sloučeniny
* Reakce vodíku s kyslíkem se nazývá hoření a jejím produktem je voda, H
2O. Další sloučeninou těchto prvků je peroxid vodíku H
2O
2, látka se silnými oxidačními účinky.
* S dusíkem tvoří čpavek neboli amoniak, NH
3, a hydrazin, N
2H
4.
* Atom vodíku je složkou každé kyseliny. Ve vodě se odštěpuje jako ion H
+ a následně vytvoří oxoniový kation H
3O
+.
* V mocenství H- tvoří vodík sloučeniny s kovy, nazývané hydridy.
* Jako jeden ze základních kamenů všech organických molekul je přítomný ve všech tkáních živých organizmů této planety.
* Zajímavou vlastností vodíku je jeho schopnost rozpouštět se v některých kovech, např. v palladiu.
Výroba a využití
Průmyslově se dnes vodík vyrábí elektrolýzou vody nebo rozkladem zemního plynu.
Hlavní využití elementárního vodíku:
* V chemickém průmyslu je vodík hydrogenačním činidlem, sloužícím k sycení násobných vazeb organických molekul, např. při ztužování rostlinných olejů.
* Redukčních vlastností plynného vodíku se někdy využívá v metalurgii k získávání kovů z jejich rud. Tento proces je ovšem nasazován pouze tehdy, kdy nelze využít běžnější redukční činidla, jako např. koks nebo dřevěné uhlí. Je to jednak kvůli poměrně vysoké ceně vodíku, ale především s ohledem na riziko možného výbuchu vodíku při kontaminaci prostředí kyslíkem nebo vzduchem za vysoké teploty.
* Vodík jako zdroj energie přestavuje pravděpodobně budoucnost energetiky i dopravy. Při spalování vodíku vzniká vedle značného energetického zisku pouze ekologicky naprosto nezávadná voda. Automobilové motory na bázi spalování plynného vodíku jsou v současné době předmětem intenzivního výzkumu předních světových výrobců motorů.
* Významnou novinkou posledních několika let je zdokonalení a zlevnění palivového článku. V tomto energetickém zařízení dochází k přímé přeměně energie chemické reakce vodíku s kyslíkem na elektrickou energii. Jako paliva se přitom používá plynného vodíku, kyslík je dodáván z atmosféry jako při normálním hoření. Účinnost tohoto procesu dosahuje v současné době hodnoty 60 %, což je podstatně více než bychom dosáhli spalováním vodíku a následným využitím vzniklého tepla pro výrobu elektrické energie. Nevýhodou současných palivových článků je stále ještě jejich vysoká cena a fakt, že proces je doposud značně citlivý vůči katalytickým jedům a vyžaduje proto použití velmi čistých chemikálií. Proto se palivové články už od šedesátých let 20. století využívají především v kosmických technologiích, kde uvedené nevýhody nejsou příliš významné.
* Perspektivně jsou izotopy vodíku pokládány za hlavní energetický zdroj při využití řízené jaderné fúze, kdy lze slučováním lehkých atomových jader dosáhnout velmi významného energetického zisku. V současné době je však tento enegetický zdroj pouze ve stádiu experimentálních prototypů a jejich zavedení do reálné praxe lze očekávat v horizontu několika dalších desítek let. Praktického využití jaderné fúze se doposud uskutečnilo pouze při výrobě termonukeární bomby a lze jen doufat, že experimenty vedené tímto směrem nebudou dále pokračovat.
Výbuch vzducholodi Hindenburg
Hoření, neboli reakce kyslíku s vodíkem je silně exotermní a lze při ní dosáhnout teplot přes 3 000 °C. Toho se běžně využívá při svařování nebo řezání kyslíko-vodíkovým plamenem nebo v metalurgickém průmyslu při zpracování těžko tavitelných kovů.
Mimořádně nízké hustoty plynného vodíku se dříve využívalo v letectví k plnění vzducholodí a balónů. Náhrada výbušného vodíku inertním heliem byla prakticky využitelná pouze v severní Americe s přírodními zdroji podzemního helia. Navíc se helium v době mezinárodního napětí stalo předměten obchodního embarga především pro vývoz do Německa. Katastrofa vzducholodi Hindenburg v roce 1937, která shořela při přistání s několika desítkami obětí, éru vodíkem plněných dopravních prostředků lehčích než vzduch definitivně skončila.
Izotopy vodíku
Vodík má 3 izotopy:
Vodík
Klasický atom vodíku (někdy nazývaný protium), tvořený jedním protonem a jedním elektronem. Tento izotop je nejjednodušší atom ve vesmíru a tvoří jeho převažující část.
Deuterium
Atom s jádrem
2H, který obsahuje v jádře jeden proton a jeden neutron a od běžného vodíku se liší především atomovou hmotností, která činí 2,01363 amu, se označuje jako deuterium. Někdy mu bývá přiřazována i chemická značka D, přestože se nejedná o jiný prvek.
Deuterium je stabilní izotop, který nepodléhá radioaktivní přeměně. V přírodě se běžně vyskytuje namísto lehkého vodíku. V průměru připadá na jeden atom deuteria 7 000 atomů normálního vodíku.
Ve spojení s kyslíkem tvoří deuterium tzv. těžkou vodu, D
2O. Tato sloučenina má významné využití v jaderném průmyslu. Je velmi účinným moderátorem, tedy látkou zpomalující rychlost neutronů. Této vlastnosti se již od druhé světové války využívá v určitém typu jaderných rektorů k přípravě plutonia z uranu.
Německá armáda se za druhé světové války intenzivně snažila vyvinout jadernou bombu na bázi plutonia. V norském Rjukanu existoval průmyslový komplex společnosti Norsk Hydro, vyrábějící těžkou vodu. Spojenci tento komplex zničili operací zvláštních jednotek (bombardování po jeho opravě způsobilo těžké ztráty na životech místních obyvatel, ale továrnu poškodilo jen mírně), přesto se však nacistům podařilo vyrobit dostatečné množství těžké vody pro další experimenty s jadernou zbraní.
Dnes je deuterium využíváno také jako účinný stopovač biochemických reakcí. Pokud je na počátku výzkumu distribuce určité sloučeniny v organizmu použita látka, která má atomy vodíku nahrazeny deuteriem, lze vysledovat její cestu biochemickou přeměnou analýzou všech možných vzniklých produktů.
Tritium
Jako tritium se označuje vodík
3H, který má jádro složeno z jednoho protonu a 2 neutronů a bývá někdy označován chemickou značkou T. Jeho atomová váha má hodnotu 3,01605 amu.
Na rozdíl od deuteria je jádro tritia nestabilní a rozpadá se s poločasem rozpadu 12,4 roku za vyzáření pouze málo energetického beta záření.
V přírodních podmínkách vzniká tritium především v horních vrstvách atmosféry při kolizi kosmického záření s jádrem atomu deuteria. Uměle je tritium získáváno v těžkovodních jaderných reaktorech při výrobě plutonia z přírodního uranu. Tritium slouží přitom jako jedna ze složek náplně ternonukleární bomby, doposud nejničivějšího destrukčního prostředku, jaký druh Homo sapiens vyrobil.
Tritium je také jedním ze základních meziproduktů jaderné fúze, která je pokládána za energetický zdroj všech hvězd v pozorovatelné části vesmíru.
Tritium se též v některých případech používá pro výrobu svítících ručiček a indexů hodinek, které pak září celou noc bez ohledu na to, zda byly před tím vystaveny světlu. Zde se tritium využívá jako zářič, který pak budí některou luminiscenční látku ke světélkování. S ohledem na poločas rozpodu tritia je životnost takové světélkující barvy řádově několik desítek let. Zdravotní rizika jsou na rozdíl od luminiscenčních barev, u kterých se používalo radium, nulové. Tritium však je používáno jen několika výrobci, protože výroba je dost nákladná. Tritium musí být vázáno jako plyn do mikrogranulí, nebo je obsaženo ve skleněných mikrotrubičkách. Obojí je technologicky náročné.








